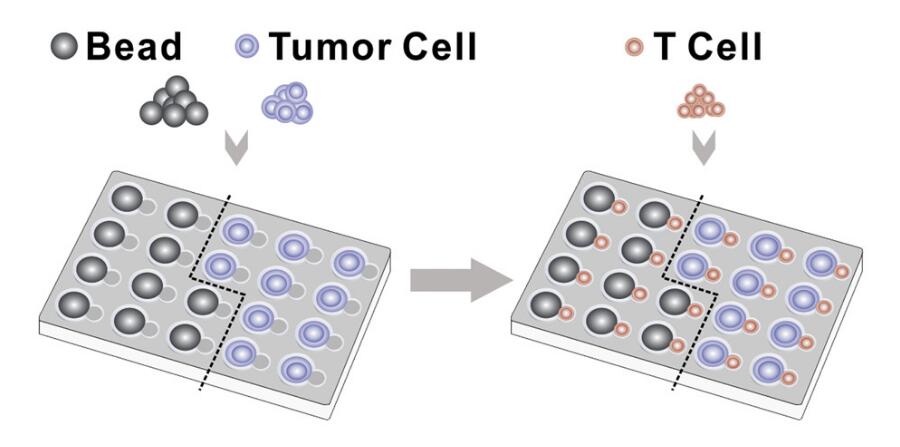
一种分层装载的微孔芯片用于排列多个细胞和功能化小珠,以形成高通量的单细胞/小珠精度的微孔阵列。
Introduction
免疫治疗近年来彻底改变了癌症治疗。作为癌症免疫治疗的一个重要分支,过继细胞转移(adoptive cell transfer, ACT)在黑色素瘤,乳腺癌,结肠癌,B细胞白血病和淋巴瘤的治疗中显示出令人印象深刻的临床反应率。
ACT治疗中,肿瘤反应性T细胞从患者自身的肿瘤组织或血液中分离出来,在有或没有受体工程的情况下,在体外大量扩增,然后注入患者体内,以介导癌症的持久消退。越来越多的证据表明,来自同一患者的不同T细胞在功能上可能不同,并导致患者的不同结果。因此,有必要在注入前对单个T细胞的功能和抗原特异性进行评估和表征。然而,传统的全群体测量可能掩盖单细胞行为和一些重要的功能异质性。例如,在肿瘤浸润淋巴细胞(TILs)群体中,只有一小部分T细胞具有肿瘤反应性。因此需要对T细胞在单细胞分辨率上进行多参数分析。
细胞因子分泌、细胞毒性和抗原特异性是T淋巴细胞的主要功能特征。为此作者开发了一个分层装载的微孔芯片,以高通量方式根据需要有效地对齐多个不同类型和/或微珠的细胞。
海拉细胞:宫颈癌细胞系。
Figure 1. Fundamental Working Principles of the Hierarchical Loading Microwell Chip

- (A)双孔HL-Chip的装载过程示意。
- (B)小珠分级装载的双孔HL-Chip单元的代表性的扫描电镜图。
- (C)小珠分级装载的三孔HL-Chip单元的代表性的扫描电镜图。
- (D)中心为大孔的HL-Chip单元的代表性的扫描电镜图。
- (E)一大块装载小珠的双孔HL-Chip的代表性的扫描电镜图。
Figure 2. Optimized Performance of the HL-Chip for Trapping Bead-Cell Pairs, Cell-Cell Pairs, and Cell-Cell-Bead Pairs

- (A)小珠-细胞对的装载效率。
- (B)小珠-细胞对的明场与荧光的代表性叠加图。
- (C)细胞-细胞对的装载效率。
- (D)细胞-细胞对的代表性叠加图。
- (E)细胞-细胞-小珠对的装载效率。
- (F)细胞-细胞-小珠对的代表性叠加图。
- (G)细胞-细胞-小珠对的大块叠加图,装载和配对效率(被占据的孔/全部孔)是从至少3次独立装载试验中随机挑选的3个显微视野(单元>400)。
Figure 3. CD-Chip for High-Throughput Detection of Cytokine Secretion from Single Lymphocytes

- (A)携带抗体的小珠接近含有T细胞的微孔,短暂共培养在开放环境,随后原位被染色标签抗体或TSA检测。
- (B)芯片上PMA/iono或DMSO刺激后4小时的IFN-γ检测的明场或绿色荧光图。
- (C)芯片上PMA/iono或DMSO刺激TILs后2、4、8小时后,独立小珠的平均荧光强度(Mean fluorescence intensity,MFI)分布。点线为部分(MFI>102)和大量(MFI>102.9)释放的阈值。
- (D)芯片上孵育8小时后,将主动分泌的克隆TILs计数。专门识别突变肽的TIL克隆在芯片外进行了8小时的预处理。
- (E)ICS和CD-Chip的相关性分析。
酪酰胺信号放大(Tyramide signal amplification,TSA)的主要原理是利用Tyramide的过氧化物酶反应(酪胺盐在HRP催化H202下形成共价键结合位点),产生大量的酶促产物,该产物能与周围的蛋白残基(包括色氨酸、组氨酸和酪氨酸残基)结合,这样在抗原-抗体结合部位就有大量的生物素沉积,与随后加入的Streptavidin—HRP/荧光基团结合,经几次这样的循环放大,可以结合大量的酶分子or荧光基团,结果使其检测信号得到几何级放大。

PMA:佛波醇酯类多克隆刺激剂,是DAG(二酯酰甘油)的类似物,脂溶性,自由通过细胞膜,直接作用于细胞活化信息传导通路上的PKC。
Ionomycin:钙离子载体,使细胞内Ca 2+浓度增加,激活calcineurin(钙调磷酸酶)。
来自PKC和calcineurin的共同信号最终引起T细胞活化。
Figure 4. Single-Cell On-Chip Cytotoxicity Assay Using Dual-Well HL-Chips
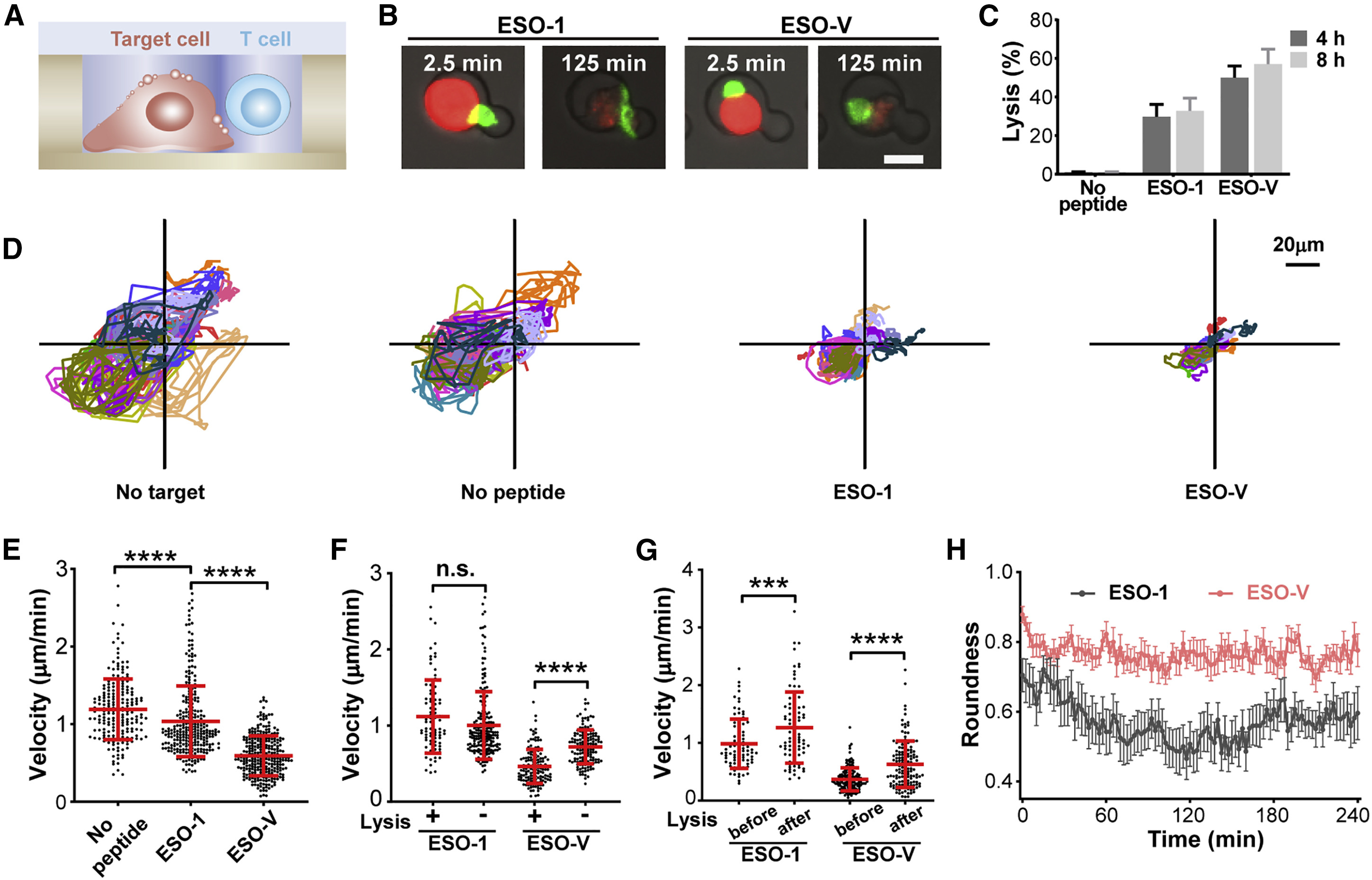
- (A)由NY-ESO-1 TCR-T细胞介导的对肽冲击的PC3/HLA-A2细胞的细胞毒性示意图。
- (B)由NY-ESO-1 TCR-T细胞介导的对肽冲击的PC3/HLA-A2细胞的细胞毒性显微图。
- (C)无肽冲击、NY-ESO-1157–165肽冲击、NY-ESO-V157–165肽冲击4或8小时的单NY-ESO-1 TCR-T细胞-靶细胞对的溶解率。
- (D)NY-ESO-1 TCR-T细胞在缺少靶细胞、与一个靶细胞成对在无肽冲击及与指定肽冲击的下的轨迹。每个轨迹展示了15条随机挑选的轨迹。
- (E)微孔中没有肽冲击(n = 221)、NY-ESO-1157–165肽冲击(n = 282)和NY-ESO-V157–165肽冲击(n = 285)下与靶细胞成对的NY-ESO-1 TCR-T细胞的平均速度。
- (F)指定肽冲击的与靶细胞成对的溶解和非溶解的NY-ESO-1 TCR-T细胞的平均速度。
- (G)指定肽冲击的与靶细胞成对的溶解前后的NY-ESO-1 TCR-T细胞的平均速度。
- (H)20个随机挑选的指定肽冲击的与靶细胞成对的NY-ESO-1 TCR-T细胞的圆度。
Figure 5. Integrated Single-Cell Analysis of Immediate Cytotoxicity and Short-Term Cytokine Secretion along with Interaction Patterns

- (A)用于同时检测细胞毒性和细胞因子分泌的检测方法图解。
- (B)显微图像下,NY-ESO-1 TCR-T细胞(蓝绿色)介导的肽脉冲的PC-3/HLA-A2(红色)细胞的细胞溶解作用,通过明显降低的荧光和形态变化来监测。孵育8小时后检测到IFN-γ。
- (C)IFN-γ分泌的热图由最大到最小对齐及NY-ESO-1 TCR-T细胞对NY-ESO-1157–165肽冲击(n = 305)和NY-ESO-V157–165肽冲击(n = 329)的靶细胞的细胞溶解活性。
- (D)NY-ESO-1 TCR-T细胞-PC-3/HLA-A2细胞相互作用的阶段分类。
- (E)不同功能组之间阶段持续时间的比较。每列代表单个靶细胞-T细胞-小珠三联体(顶部,NY-ESO-1157–165肽冲击(n = 305);底部,NY-ESO-V157–165肽冲击(n = 329)),其中相应的阶段持续时间成比例地映射到柱上。
Discussion
相比传统的评估方法,本方法有四大优势:
- 具有细胞活性和可挽救性、实时检测的优点。
- 通过开放的结构,可以取回单个细胞供整合芯片上方法和芯片外的后续分析包括特定细胞的基因和转录分析。
- HL-Chip提供了高通量和单细胞装载效率,且便于操作。
- HL-Chi提供了单个T细胞分泌、细胞毒性和细胞行为的同时检测,可以提供更全面的T细胞评估。
Reference
Zhou Y, Shao N, Castro R B de, et al. Evaluation of Single-Cell Cytokine Secretion and Cell-Cell Interactions with a Hierarchical Loading Microwell Chip[J]. Cell Reports, Elsevier, 2020, 31(4).